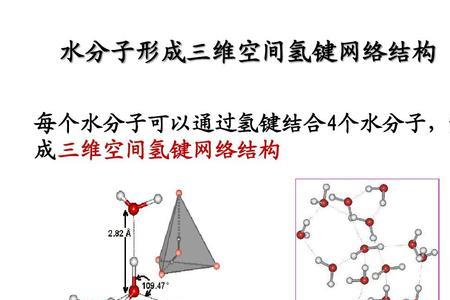
判断分子的空间构型,常用的方 法有3种。
—、价层电子对互斥模型(VSEPR)
早在1940年,希吉维克和坡维尔在总结实验事实的基础上提出了一种简单的理论模型,用以预测简单分子或离子的立体 结构.这种理论模型后经吉列斯比和尼霍尔姆在20世纪50年发展而来。
二、杂化轨道理论
国化学家鲍林于1931年提出了杂化轨道理论,轨道杂化是指不同类型、能量相近的原子轨道,在形成分子的成键过程中重新组合成一系列能量相等的新的轨道。这种轨道重新组合的过程叫做杂化,所形成的新轨道称为杂化轨道
三、等电子体原理
人们研究分子结构时,根据许多类似的实验事实,总结出一 条经验规律:具有相同价电子数和相同原子数的分子或离子具有相同的结构特征,这一原理称为“等电子体原理”。这里的“结 构特征”既包括分子的立体构型,又包括化学键的类型,但键角 并不一定相等.
分子空间结构判断方法
1、组成元素:
有活泼金属或nh4+构成的化合物一般为离子晶体
原子晶体比较特殊,如:金刚石、晶体硅、碳化硅、二氧化硅重点记
其余一般为分子晶体
2、化学键分析:
只要有离子键即为离子晶体
全部都是共价键为原子晶体
存在分子间作用力为分子晶体
3、熔沸点等物理性质分析:
一般情况:原子晶体>离子晶体>金属晶体>分子晶体
其他特殊情况特殊记
晶体简介:
1、离子晶体:阴、阳离子以一定的数目比、并按照一定的方式依靠离子键结合而成的晶体。
如“nacl、cscl
构成晶体的微粒:阴、阳离子
微粒间相互作用:离子键
物理性质:熔点较高、沸点高,较硬而脆,固体不导电,熔化或溶于水导电。
2、原子晶体:晶体内相临原子间以共价键相结合形成的空间网状结构。
如:金刚石、晶体硅、碳化硅、二氧化硅
构成晶体的微粒:原子
微粒间相互作用:共价键
物理性质:熔沸点高,高硬度,导电性差。
3、分子晶体:通过分子间作用力互相结合形成的晶体。
如:所有的非金属氢化物,大多数的非金属氧化物,绝大多数的共价化合物,少数盐(如alcl3)。
构成晶体的微粒:分子
微粒间相互作用:范德华力
物理性质:熔沸点低,硬度小,导电性差。