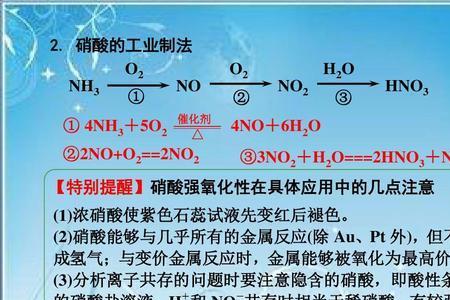
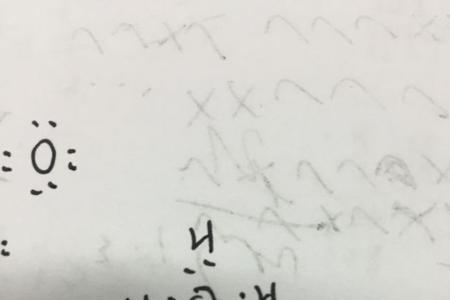化学式HNO2。亚硝酸仅存在于稀的水溶液中,是一种弱酸,不稳定,易分解成NO2和NO,也能发生如下歧化反应:
3HNO2─→HNO3+2NO+H2O
在亚硝酸中氮原子的氧化数是+3,是一种中间氧化态,因此,亚硝酸既具有氧化性,又具有还原性,而氧化性比还原性更为突出。例如,它在水溶液中能将I-离子氧化为单质碘:
2HNO2+2I-+2H+─→I2+2NO+2H2O
这个反应可用于分析测定。在多数的情况下,亚硝酸可还原成氧化氮NO,也可还原成氧化二氮N2O、氮、胲NH2OH或氨NH3。它被氧化时,即成为硝酸。
将二氧化氮和氧化氮的混合物溶解在接近零度的水中,即生成亚硝酸的水溶液:
NO2+NO+H2O─→2HNO2
在亚硝酸盐溶液中加入酸,也可得到亚硝酸的溶液:
NaNO2+HCl─→HNO2+NaCl
亚硝酸在工业上用于有机合成,使胺类转变成重氮化合物,从而制备偶氮染料。
亚硝酸与碳酸化学式怎么写
亚硝酸的化学式HNO2碳酸的化学式H2CO3
亚硝酸是N(III)对应的含氧酸,是一种弱酸,电离平衡常数Ka=6.0E-4,只能存在于很稀的冷溶液中,溶液浓缩或加热时,就分解成H2O和N2O3,后者又会分解成NO2和NO。用于制染料、药物,并用作试剂。
碳酸(H₂CO₃)是一种二元弱酸,电离常数都很小。但也有认为其为中强酸,因为根据无机酸酸性强弱判断式(OH)nROm可判断其酸性与磷酸相似。在常温、常压下,二氧化碳饱和溶液的浓度约为0.033mol/L,pH为5.6,pKa=6.37。