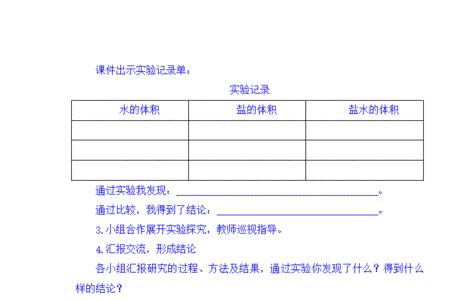
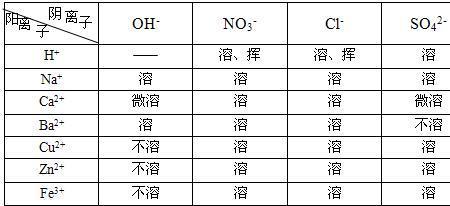
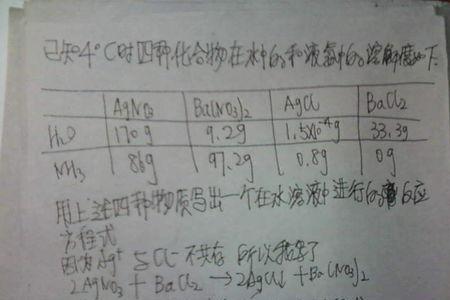
溶解度S/100g=溶质质量/溶剂质量,溶解度S=100g*溶质质量/溶剂质量,饱和溶液溶解度S 和溶质质量分数 w 的互算,S=100g*w/(1-w),w=S/(100g+S)*100%。
在一定温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的溶质的质量,叫做这种物质在这种溶剂中的溶解度。
溶解度原理
溶解度是化合物在与其固相处于平衡状态时在溶剂介质中所能达到的最高浓度。
化合物并没有单一的溶解度值,溶解度取决于许多因素∶
化合物结构
溶液中引入化合物的物理状态
- 固态∶无定形、晶体、多晶型
- 液态∶预溶于溶剂中,例如二甲基亚砜(DMSO)
溶剂的组成和物理状态
- 溶剂的种类
- 助溶剂的含量(%)
- 溶液成分(例如盐、离子、蛋白质、脂类、表面活性剂)
- pH
- 温度
溶解度原理
溶解的本质是聚集在一起的分子集团或原子集团被另一种分子集团或原子集团所打破形成了一种新的分散系的过程.值得强调的是,有的溶解仅是物理变化,如蔗糖溶于水
但有的溶解则是化学变化,如NACL溶于水,NACL晶体之间的强烈的离子键被水分子所破坏,变成了水和氢离子,水和氯离子还有的则是既有化学变化有有物理变化,如乙酸,乙酸溶与水后,先由聚集在一起的状态分成单个分子的状态(此过程跟氢键也有关),然后在电离成水合醋酸根离子和水合氢离子.一般自然界中第三种情况居多,因为自然界的大部分物质是有机物.