碳的原子半径小于硅原子半径。因为碳是6号元素,原子核外有2个电子层,最外层上有4个电子。而硅是14号元素,原子核外有3个电子层,最外层上有4个电子。二者最外层电子数相同,都位于元素周期表第四主族。但硅核外多一个电子层,所以原子半径C<Si。

碳和硅原子半径大小
原创 | 2022-12-17 12:04:30 |浏览:1.6万
猜你想问
-
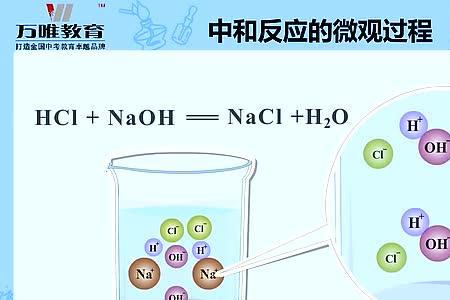 一氧化碳和碱反应的区别 二者不反应,无法说出区别。一氧化碳(CO)为非金属氧化物,碱是由金属离子和氢氧根离子构成的化合物,如氢氧化钠(NaOH),在非金属氧化物与碱之间可以发生复分解反应,但复分解反...
一氧化碳和碱反应的区别 二者不反应,无法说出区别。一氧化碳(CO)为非金属氧化物,碱是由金属离子和氢氧根离子构成的化合物,如氢氧化钠(NaOH),在非金属氧化物与碱之间可以发生复分解反应,但复分解反... -
 比较四氯化碳和甲烷的偶极矩 尽管C-H/C-Cl是极性键,但它们都是非极性分子,因为分子结构对称(C原子位于正中,其它原子构成正四面体的顶点),偶极矩都为0.不过这是平均情况.对于单个或个别的分子而言,由...
比较四氯化碳和甲烷的偶极矩 尽管C-H/C-Cl是极性键,但它们都是非极性分子,因为分子结构对称(C原子位于正中,其它原子构成正四面体的顶点),偶极矩都为0.不过这是平均情况.对于单个或个别的分子而言,由... -
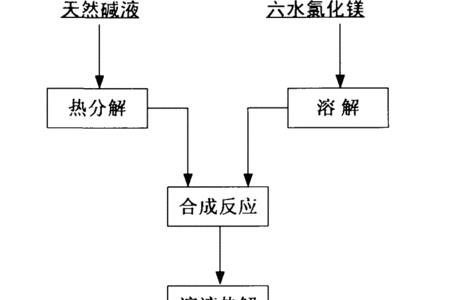 二氧化碳和镁为啥不生产碳酸镁 镁和二氧化碳反应没有生成碳酸镁,因为氧原子不够,二氧化碳碳氧比为2:1,而碳酸根碳氧比为1:3,氧原子不够,所以不可能生成碳酸镁,只能从二氧化碳里面里面夺取一个氧原子,与镁...
二氧化碳和镁为啥不生产碳酸镁 镁和二氧化碳反应没有生成碳酸镁,因为氧原子不够,二氧化碳碳氧比为2:1,而碳酸根碳氧比为1:3,氧原子不够,所以不可能生成碳酸镁,只能从二氧化碳里面里面夺取一个氧原子,与镁... -
 金麒麟高碳和陶瓷刹车片哪个好 陶瓷刹车片好。陶瓷刹车片可谓弥补了有机型和半金属型刹车片的不足。它的材质主要是由矿物纤维、芳纶纤维以及陶瓷纤维等多种材质组合而成。一方面,由于没有金属材...
金麒麟高碳和陶瓷刹车片哪个好 陶瓷刹车片好。陶瓷刹车片可谓弥补了有机型和半金属型刹车片的不足。它的材质主要是由矿物纤维、芳纶纤维以及陶瓷纤维等多种材质组合而成。一方面,由于没有金属材... -
 cj麦科勒姆有碳和反伍2谁更好 反伍2更好一些。李宁反伍2适合大体重选手,此前李宁推出的反伍1代就非常适合大体重选手,这一系列球鞋就是专为大体重球员而生的。反伍2中底搭载flight foam和前后掌...
cj麦科勒姆有碳和反伍2谁更好 反伍2更好一些。李宁反伍2适合大体重选手,此前李宁推出的反伍1代就非常适合大体重选手,这一系列球鞋就是专为大体重球员而生的。反伍2中底搭载flight foam和前后掌...
