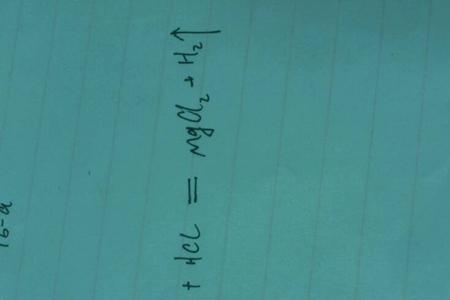氯化钙溶液和硫酸不能发生反应。CaCl2+H2SO4=CaSO4+HCl无沉淀气体水生成因为复分解的实质是离子浓度减小沉淀不水解水。
氯化钙溶液和硫酸的离子方程式
离子方程式:
Ca2⁺+2Cl⁻+2H⁺+SO4(2⁻)=CaSO4
+2HCl (气)
氯化钙溶液和硫酸,当两者浓度小时,不反应,两者均为浓溶液时,可反应:
CaCl2+H2SO4(浓)=CaSO4+2HCl (气)
应该是有白色盐酸气体。
离子方程式:
Ca2⁺+2Cl⁻+2H⁺+SO4(2⁻)=CaSO4
+2HCl (气)
当两者的浓度比较小时是不反应的,钙离子和硫酸离子的浓度子超过硫酸钙的溶度积常数,所以不会有硫酸钙沉淀。但两者都是浓溶液时,就能发生沉淀,因为当两者浓度足够大,说明钙离子和硫酸离子的浓度积就会超过硫酸钙的溶度积常数,就会有硫酸钙沉淀。也可以从硫酸钙微溶于水的事实出发而推得上面的结论。