会氮气反应。
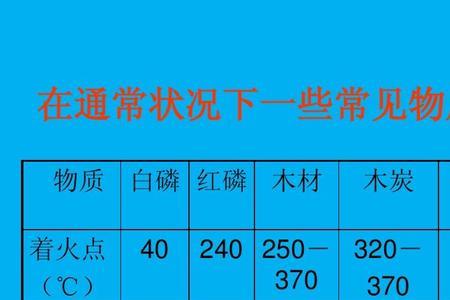
白磷是一种磷的单质,化学式为P4。外观为白色或浅黄色半透明性固体。质软,冷时性脆,见光色变深。暴露空气中在暗处产生绿色磷光和白烟。在湿空气中约40℃着火,在干燥空气中则稍高。
白磷能直接与卤素、硫、金属等起作用,与硝酸生成磷酸,与氢氧化钠或氢氧化钾生成磷化氢及次磷酸钠或磷
白磷是否会与氮气反应
白磷不会与氮气反应,可熄灭白磷。
液态的氮气是无色,无臭,无腐蚀性,不可燃,温度极低,化学性质稳定,气化时会吸收大量热量,液氮必须储存在专用的液氮罐中,把液氮倒进着火点,火焰会立刻冷却下来而熄灭,当然,理论上来讲可以熄灭白磷。但液氮不能用于灭火,其原因如下
1、液氮灭火器非常昂贵,一场火造成的损失可能还不如用液氮灭火器的损失大,而且灭火剂只可保存48小时。
2、液氮气化时会释放大量氮气,氮气可以隔绝外部的氧气。
3、液氮很难保存,可能撒上去还没到火点就蒸发了,起不到效果。
4、要把氮气压缩到液态,至少需要数百个大气压的容器,而且大量释放的时候,会引起灭火人员缺氧窒息。
白磷是否会与氮气反应
不对。
“常温下白磷可自燃而氮气须在放电时才与氧气反应“这个实验事实只能说明P4的非金属性大于N2的金属性,而不能说明N,P两元素的性质
本来N的电子层数比P少,非金属性本应更强
但在N2,有氮氮三键这种稳定的结构,因而很稳定,体现不出氧化性