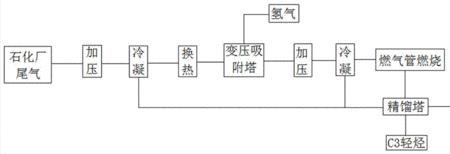
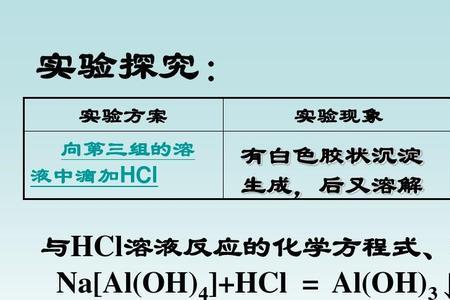
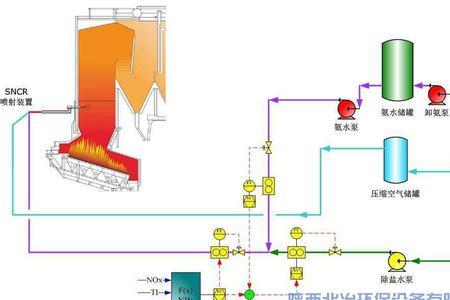
氢气(H2)为气态非金属单质,制取它的反应原理有:
①给水通电,发生分解反应,方程式:2H2O=(通电)2H2↑+O2↑。
②让比氢元素活动性强的金属单质与酸发生置换反应,如:Fe十2HCI=FeCl2十H2↑。Zn十H2SO4=ZnSO4十H2↑或者Mg十2HNO3=Mg(NO3)2+H2↑等。
制氢气的反应原理
实验室一般用锌粒与盐酸或稀硫酸反应制取氢气。
化学方程式如下:
使用盐酸
Zn+2HCl=ZnCl2+H2↑
使用稀硫酸
Zn+H2SO4=ZnSO4+H2↑
制氢气的反应原理
实验室制取氢气的反应原理是:Zn+H2SO4=ZnSO4+H2↑实验室里通常用稀硫酸跟金属锌起反应来制取氢气,也可以用盐酸代替硫酸,用镁或铁代替锌来制取氢气。