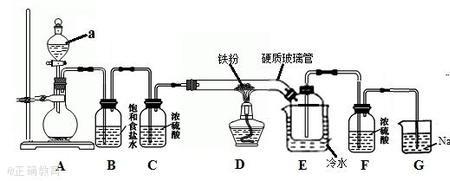
这是因为在溶液中,氢离子的氧化性强于亚铁离子,但是却弱于铁离子。因此盐酸中的氢离子只能将铁单质氧化成弱于它的亚铁离子,而不能将其氧化成强于它的铁离子。
该反应化学反应式为:Fe+2HCl==FeCl₂+H₂↑
离子反应式为:Fe+2H⁺==Fe²⁺+H₂↑
氯化亚铁,化学式FeCl2。呈绿至黄色。可溶于水、乙醇和甲醇。溶于水、乙醇、乙酸,微溶于丙酮,不溶于乙醚。氯化亚铁溶液为浅绿色溶液,在空气中会逐渐氧化成氯化铁。
为什么氯化氢和铁生成氯化亚铁
题中问的是:为什么氯化氢和铁生成氯化亚铁
Fe和HCI的反应是置换反应,同时也是氧化还原反应。在这个反应中,H+作氧化剂,Fe作还原剂。
阳离子的氧化性从强到弱的顺序:
Ag+>Hg(2+)>Fe(3+)>Cu(2+)>H+……>Fe2+
氧化还原反应必须满足:
氧化剂的氧化性>氧化产物的氧化性
如果生成Fe(3+),Fe(3+)的氧化性>H+,违背了氧化还原反应的规律,因此只能生成Fe(2+),满足了:氧化性,H+>Fe(2+)