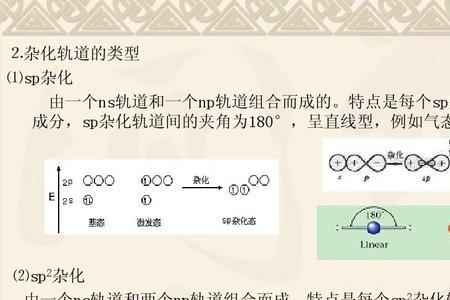
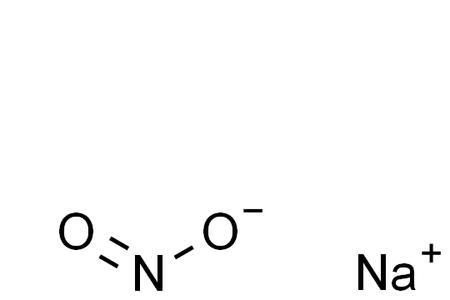
硝酸中N为sp2杂化,与3个O形成3个σ键,还有一个π46,(4原子6电子π键)可以激发,通常2个轨道的能量相差不是很大就可以激发,重组并杂化,2s和2p能量差别不是很大,二者经常杂化,如CH4中,C就是2s与3个2p组合杂化成4个sp3杂化轨道
硝酸(英文名:Nitric acid),是一种具有强氧化性、腐蚀性的一元无机强酸,是六大无机强酸之一,也是一种重要的化工原料,化学式为HNO3,分子量为63.01,其水溶液俗称硝镪水或氨氮水。
硝酸中氮原子的杂化方式
N原子价电子排布是2s2 2p3 NO3-中N原子采取sp2杂化,未参与杂化的p轨道上成单电子,且与三个氧原子的pz轨道平行重叠,形成一个四中心五电的子离域π键。所以硝酸根的空间构型是平面三角形。