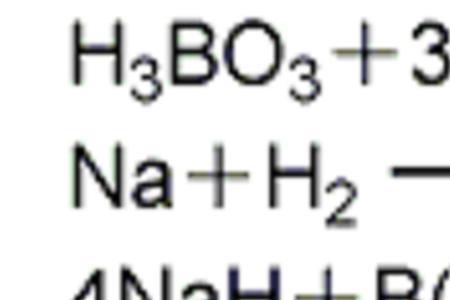一般是强碱,如,NaOH、KOH、Ca(OH)2、Ba(OH)2。
碱溶液能与酸碱指示剂作用:碱溶液遇紫色石蕊试液变蓝(现象不明显,但有变化),遇无色酚酞溶液变红(现象明显)。
碱能与非金属单质发生反应:氯气与碱的歧化反应,如:Cl2+2NaOH=NaCl+NaClO+H2O (Br2、I2类等)。
四种易溶于水的碱的化学式
一般是强碱,如,NaOH、KOH、Ca(OH)2、Ba(OH)2
这是初中要记忆的4个
除此之外,有一个特例,弱碱,NH3.H2O,一水合氨
强碱是指在水溶液中电离出的阴离子全部是氢氧根离子的物质。强碱与酸反应形成盐和水。所谓强碱、弱碱是相对而言,碱溶于水能发生完全电离的,属于强碱。碱金属和部分碱土金属对应的碱一般是强碱。其溶液在标准情况下(浓度为0.1mol/L)的pH>12。
四种易溶于水的碱的化学式
氢氧化钠NaOH
氢氧化钾KOH
氢氧化钙Ca(OH)2
氢氧化钡Ba(OH)2
氨水NH3·H2O