1、单质密度之比1:2:3 密度=质量/体积 在标况下(三种同位素均为气体) 取同体积的三种同位素 质量只与它们的摩尔质量有关,也就是是他们的摩尔质量之比1:2:3。(标况下 气体质量=摩尔质量*22.4L/mol*体积)
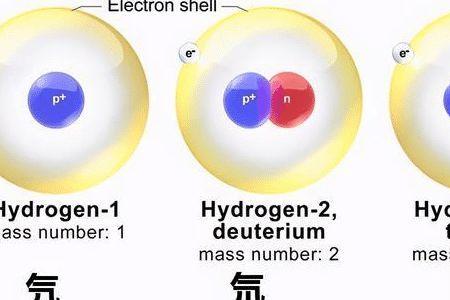
2、质子数之比1:1:1 同种元素所有的同位素所含的质子数均相等。
3、1g单质中它们的中子数之比0:3:4 它们的相对原子质量分别为1,2,3。所以一g中他们分别有1mol,0.5mol,1/3mol 氕不含中子,氘含一个,氚含两个。中子之比为0:1/2:2/3=0:3:4
4、电子数之比为1:1:1 电子数之比等于质子数之比,标况下1mol气体体积为22.4L/mol。1L单质中它们所含的三种元素的物质的量相等。质子数相等。