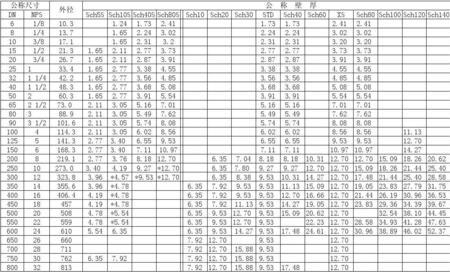
过氧化氢使高锰酸钾褪色的原理是过氧化氢具有还原性,把高锰酸钾中的高锰酸根还原成锰离子(由于过氧化氢中的氧是负一价,所以既具有氧化性也具有还原性,在化学反应时可以单独的表现出氧化性和还原性,或者既是氧化性也有还原性)。
h2o2使kmno4溶液褪色是什么原理
高锰酸钾具有强氧化性,作为氧化剂,双氧水作为还原剂,把高锰酸钾还原为二氧化锰黑色沉淀和一些其他价态的锰离子。具体的要看反应是在什么条件下的(如酸性、碱性、中性)
2mno4-+5h2o2+6h+=2mn2++5o2↑+8h2o利用此反应可测定h2o2的含量。滴定时加入kmno4的速度不能太快,否则易产生mno2沉淀,mno2又可促进h2o2的分解,增加测定误差。滴入第一滴kmno4溶液时不易褪色,待mn2+生成后,由于mn2+的催化作用,加快了反应速度,测定速度也随之加快,一直滴定到呈现稳定的微红色,即为终点。