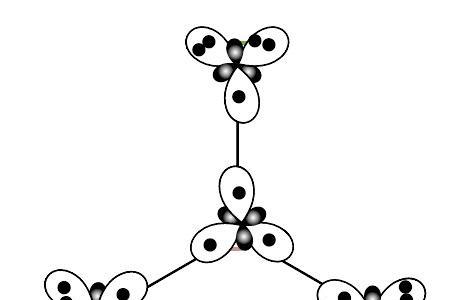
由于硼是缺电子结构,三氟化硼形成一个4中心6电子的大π键,6个电子分别由3个氟原子提供,3个氟原子各提供1个全充满的2p轨道,与硼原子的空p轨道肩并肩,形成大π键。B原子以sp2杂化轨道成键,分子为平面正三角形分子。
硼为啥能有四个键
一般的是3个,比如BCl3
但在硼烷、配合物中,也可以是4个
因为硼形成3个共价键后,还有1个空轨道,能接受1对电子,形成配位键,比如HBF4
B上连接4个F,其中有一个就是F→B配位键
原创 | 2022-11-14 12:07:37 |浏览:1.6万
由于硼是缺电子结构,三氟化硼形成一个4中心6电子的大π键,6个电子分别由3个氟原子提供,3个氟原子各提供1个全充满的2p轨道,与硼原子的空p轨道肩并肩,形成大π键。B原子以sp2杂化轨道成键,分子为平面正三角形分子。
硼为啥能有四个键
一般的是3个,比如BCl3
但在硼烷、配合物中,也可以是4个
因为硼形成3个共价键后,还有1个空轨道,能接受1对电子,形成配位键,比如HBF4
B上连接4个F,其中有一个就是F→B配位键




Copyright 2005-2020 www.kxting.com 版权所有 |  湘ICP备2023022655号
湘ICP备2023022655号
声明: 本站所有内容均只可用于学习参考,信息与图片素材来源于互联网,如内容侵权与违规,请与本站联系,将在三个工作日内处理,联系邮箱:47085,1089@qq.com