Fe与过量浓硫酸H2SO4反应:
2Fe+6H2SO4(热、浓)=Fe2(SO4)+3SO2(气)+6H2O
铁即Fe在常温下,遇到冷的浓硫酸,发生钝化反应。在加热条件下,铁能与浓硫酸反应发生氧化还原反应。
2Fe+6H2SO4(浓)=Fe2(SO4)3+3SO2(气)
+6H2O
随反应的不断进行,浓硫酸会变成稀硫酸Fe+H2SO4=FeSO4+H2↑
当然,因为铁不足量,该反应不一定发生
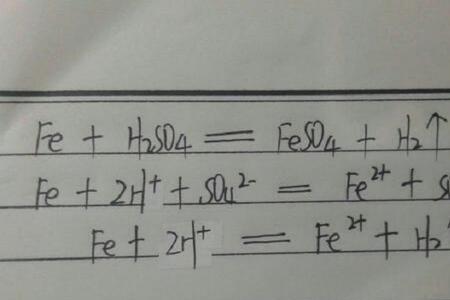
原创 | 2022-11-13 20:04:38 |浏览:1.6万
Fe与过量浓硫酸H2SO4反应:
2Fe+6H2SO4(热、浓)=Fe2(SO4)+3SO2(气)+6H2O
铁即Fe在常温下,遇到冷的浓硫酸,发生钝化反应。在加热条件下,铁能与浓硫酸反应发生氧化还原反应。
2Fe+6H2SO4(浓)=Fe2(SO4)3+3SO2(气)
+6H2O
随反应的不断进行,浓硫酸会变成稀硫酸Fe+H2SO4=FeSO4+H2↑
当然,因为铁不足量,该反应不一定发生





Copyright 2005-2020 www.kxting.com 版权所有 |  湘ICP备2023022655号
湘ICP备2023022655号
声明: 本站所有内容均只可用于学习参考,信息与图片素材来源于互联网,如内容侵权与违规,请与本站联系,将在三个工作日内处理,联系邮箱:47085,1089@qq.com