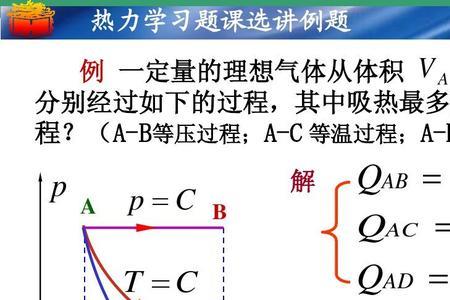
容摩尔热容直接和内能发生关系,等压摩尔热容不是一个重要的量,只是方便时使用。因为理想气体的内能
E=NCvT
所以
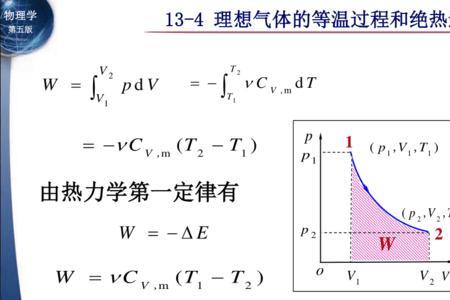
绝热过程
dW+dE=0
so
pdV+NCvdT=0
因为状态方程
pV=NRT
so
dT=[pdV+Vdp]/NR
代入就得到
(1+R/Cv)dV/V+dp/p=0
由于dE是内能的改变量,计算时,要用气体等体摩尔热容,必须确保体积不发生改变。体积发生改变会对外做功。其中等压摩尔热容C(P)=C(V)+R,即1mol的理想气体在等体过程中会多吸收R的热量,用来膨胀对外做功。恒量R=8.31J